Üdvözlet webhelyünk lakói!
Évről évre az olajtermelés egyre összetettebbé válik, és az abból nyert üzemanyag egyre drágábbá válik. Az EU országaiban általában azzal fenyegetnek, hogy abbahagyják a benzinmotorok gyártását, minden járművet elektromos autókkal akarnak kicserélni. De a lítium akkumulátorok még mindig messze vannak az ideálisól, és egyébként semmi sem siet, hogy egy ideálisvá váljanak. A legjobb esetben a lítium akkumulátor egyszeri feltöltése esetén legfeljebb 700 km távolságot lehet megtenni, amely után kb. Egy hétig kell töltenie az akkumulátort, és ha a töltéshez szokásos aljzatot használ, ez általában sok időt vesz igénybe. Képzelje el, mi történik, ha mindenki folyamatosan tölti az elektromos autóját, milyen hatalmas terhelések lesznek az elektromos hálózaton, és mekkora feszültség veszti el. Általánosságban elmondható, hogy a lítium akkumulátorok jövője továbbra is meglehetősen homályos, és évente egyre több kutatást szentelnek az új akkumulátor lehetőségek keresésének.
Mint tudod, a legtöbb energiaigényes fém az alumínium. Már korunkban az alumínium akkumulátorok prototípusainál kb. 2000 km-t megtölthetünk újratöltés nélkül, és az ilyen típusú akkumulátorok újratöltése mindössze 15 percet vesz igénybe, ezután kb. 2000 km-rel tovább haladhat.
Az alumínium akkumulátorok újratöltése különbözik a lítium-alapú akkumulátorok újratöltésétől. Ennek ellenére semmi bonyolult nincs benne, csak be kell helyeznie egy új alumíniumot, ki kell önteni az elektrolitot és be kell tölteni egy új elektrolitot, minden lényegében ugyanaz, mint a benzin egy autó, csak ez egy elektromos autó, és nincs terhelés az elektromos hálózaton. Ezen túlmenően nem kell hatalmas számú aljzatot gyártania hatalmas keresztmetszetű vezetékekkel, hogy mindezeket az elektromos autót feltöltse.
De itt nem minden olyan simán. Az alumíniumból villamosenergia-megszerzés egyáltalán nem olyan egyszerű, mint szeretnénk. Először találjuk ki, mi az alumínium-levegő akkumulátor alapelve.
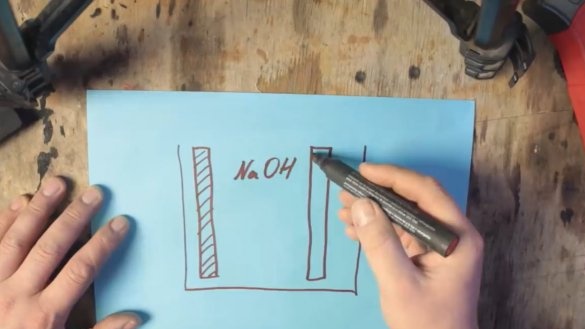
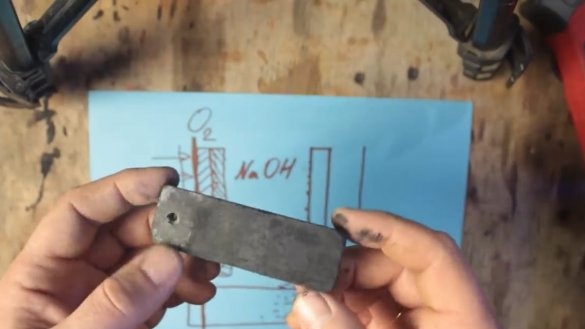
Ahhoz, hogy egy ilyen elem működjön, 2 elektródra lesz szükség: az egyik természetesen alumíniumból, a második grafitból készül. Mindkét elektróda elektrolit oldatban van.
Só (NaCl) használható elektrolitként, de ezzel a feszültséget kb. 0,7 V-ra növelheti. Az alkáli elektrolit (NaOH) feszültsége már jobban, kb. 1 V-ra emelhető.
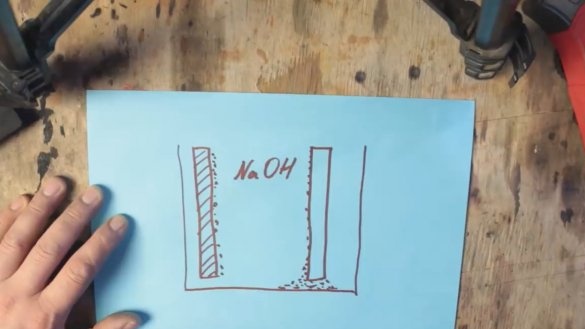
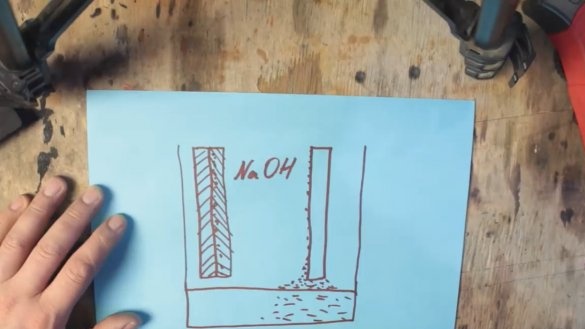
A kémiai reakció során az alumíniumot alumínium-hidroxid-réteggel (Al (OH) 3) vonják be, amely fokozatosan a tartály aljára süllyed. A grafit elektróda felületén hidrogénbuborékok alakulnak ki, amelyek viszont az ellenállás növekedéséhez és a feszültség csökkenéséhez vezetnek, ezt a folyamatot polarizációnak nevezzük.
Az alumínium-hidroxid kicsapódásával kapcsolatos első problémát úgy lehet kiküszöbölni, hogy egyszerűen megnöveljük a kiégett termék lerakódásának kapacitását, de a második problémát egy mangán-oxid alapú depolarizáló tömeg segítheti elő, amely működés közben mangán-hidroxiddá alakul.
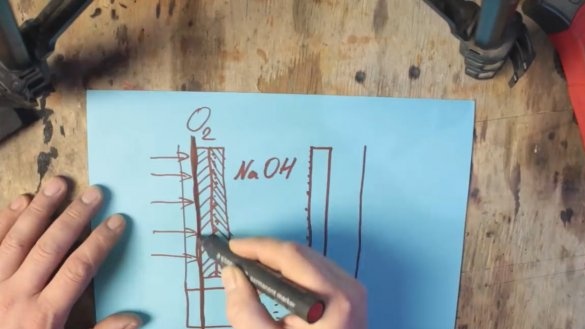
Valójában van egy közönséges alkáli elem, de csak egy nagyon nagy. De új probléma merül fel. Tény, hogy a mangán-oxidot szintén fogyasztják, és azt is meg kell változtatni. Gondoskodnunk kell arról, hogy csak alumíniumot használjunk el. Ehhez vegyen oxigént a környező levegőből. Itt kezdődik az alumínium-levegő akkumulátor. Az egyik falat csak gázáteresztő membránnal kell cserélni, a grafit elektródot pedig grafit és mangán-oxid és platina vagy ezüst nanorészecskék keverékével kell cserélni.
A nemesfém nanorészecskékkel rendelkező mangán-oxid nem reagál, hanem katalizátorként működik, amelynek eredményeként az elektrolit hidrogénje a levegőben lévő oxigénnel oxidálódik.
Az ezüst nanorészecskékkel záródó mangán-oxid előállításának technológiája elvileg nem bonyolult, és kézműves körülmények között is kipróbálható. De ebben a cikkben megvitatjuk, hogyan lehet a legtöbb költségkeretet megtenni az akkumulátor számára, amely alumínium energiát vesz fel. A következő utasításokat a Tüzes TV-csatornáról vettük át. További részletek a szerző eredeti videójában:
A grafit maximális költségvetési változata a nyári érintkezőbetétek a trolibuszok számára. A végleges trolibuszmegállókban teljesen ingyenesen találhatja meg őket, vagy meg is vásárolhatja őket, nem drágák, a szerző darabonként 22 rubelt vásárolt.
Ezután lúgra van szükségünk. Itt van egy eszköz csövek tisztítására, amelynek összetétele száz% nátriumlúgot tartalmaz.
A lúgos reakció elindításához egy kicsit szükségünk van, 1 liter lúg 0,5 l vízre elegendő.
Először is ellenőrizzük, van-e valójában grafitelektród az akkumulátorban. A tapasztalat kedvéért vegyük ezt a rozsdamentes acél elektródát.
Most az alumínium lemezt és a rozsdamentes acél elektródát tesszük az alkáliba, csatlakoztassuk a multimétert, és megnézhesük, hogy hány volt lesz.
Mint láthatja, kiderült, hogy körülbelül 1,4 V. Most ellenőrizzük a rövidzárlati áramot.
Rövidzárlati áram váltott ki 20mA tartományban. Milyen következtetéseket lehet levonni: szélsőséges körülmények között elméletileg össze lehet szerelni egy rozsdamentes acélból készült bögréket és alumíniumfóliát.
Ezután réz elektród készül, amely elektromos rézből készül.
Mint megfigyelhetjük, a feszültség kismértékben meghaladta az 1,4 V-ot, de a rövidzárási áram eleinte magas volt, de aztán meglehetősen gyorsan csökkenni kezdett, és a réz sötét bevonattal kezdett borulni, valószínűleg a víz szennyeződése okozta ezt a hatást, mivel a víz Ebben a kísérletben a szerző vett egy csapot a csapból.
Most merítse a grafit elektródot az elektrolit oldatba.
Ezzel az elektródával 1,3 V feszültséget kapunk, és a rövidzárási áram 17 mA tartományban leállt. Első pillantásra úgy tűnik, hogy a rozsdamentes acél elektróda hatékonyabb, de a rozsdamentes elektróda felülete nagyobb, tehát még nem ismert, melyik grafit vagy rozsdamentes acél jobb.
Mivel a grafit meglehetősen nagy ellenállással rendelkezik, valahogy meg kell birkóznia vele. Elektródákat kell készíteni olyan anyagból, amely jól vezetőképes, és a grafitnak csak a felületén kell lennie.Úgy döntöttek, hogy fúrnak át a grafiton, és a kapott lyukakban vágják le az M6 csavarok menetét.
Az eredmény egy acél elektróda grafithéjjal.
A nem fúrt grafit ellenállása kb. 4,5 Ohm, a fúrt grafit ellenállása pedig körülbelül 1,7 Ohm.
Az arcon az ellenállás csökkenése és ennek következtében a szerkezet hatékonysága növekszik. További kísérletekben desztillált vizet fogunk használni.
Az első kísérlet elektrolittal, amelyben 4 g lúgot tartalmaznak 1 liter vízben.
Rövidzárlati áram 150mA-ra váltott. A következő elektrolit koncentrációja 6 g lúg / liter. Nos, és így tovább, minden alkalommal növeljük a koncentrációt 2 g-mal, amíg el nem éri azt a koncentrációt, amelyen az áram nem fog növekedni.
Annak ellenére, hogy egy ilyen egyszerű akkumulátor nem rendelkezik nagy áramhatékonysággal, az ilyen akkumulátor nagyon hosszú ideig működhet, és elektródként bármilyen alumínium használható, amely bármilyen alakú elektródává könnyen elolvasztható, például alumínium kannák különféle alkoholos és alkoholmentes italok, csokoládé fólia stb.
Ennek eredményeként az összes elektrolitkoncentrációval végzett kísérlet után világossá válik, hogy az akkumulátor ilyen kivitelével nincs értelme 12 g-nál több lúgot hozzáadni 1 liter vízhez, azaz körülbelül 1% -os oldatot kapunk.
Aztán a szerző összeállított egy másik, 3 elektródából álló klipet.
Két elem nagyobb feszültséget és kevesebb veszteséget ad, így jobb az eredmény.
Vegyünk egy vödröt elektrolitot, egy nagy darab alumíniumot és 2 rozsdamentes acél elektródát.
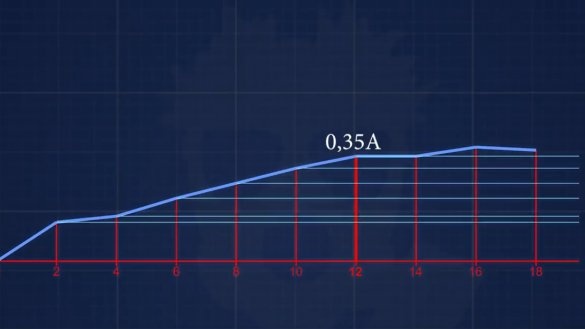
Egy vödörben elektrolitkoncentráció 10 g / 1l. Csúcsáram 1.3A, lecsökkent 520mA-ra. A rozsdamentes acél hatalmas felületével nem hasonlított össze a grafittal, mert 600 mA-nak bizonyult grafittal. Egyébként a reakció során hidrogén szabadul fel, amely összegyűjthető és energiaforrásként felhasználható. Röviden: még van hely növekedni. Most már minden. Köszönöm a figyelmet. Találkozunk hamarosan!